Adhäsion-GPCRs
Gpr126 ist ein Adhäsions G protein-gekoppelter Rezeptor (aGPCR). Damit gehört er zur großen Gruppe der sieben-Transmembran (7TM) Typ G protein-gekoppelten Rezeptoren, die sich als Dreh- und Angelpunkte für zahlreiche physiologische Funktionen herausgestellt haben. Zudem sind sie eine Fundgrube für moderne pharmazeutische Interventionen. aGPCR sind im Gegensatz zum Rest der 7TM-Rezeptorfamilie die bei weitem am wenigsten erforschte 7TM-Rezeptorklasse. aGPCRs besitzen lange N-Termini mit verschiedenen Funktionsdomänen. Darüber hinaus werden viele von ihnen autoproteolytisch (GPS Motiv) in ein N-terminales Fragment (NTF) und C-terminales Fragment gespalten. Doch weder sind die allgemeinen biologischen und pharmakologischen Eigenschaften von aGPCRs bekannt, noch wurden sie in der Biomedizin genutzt.
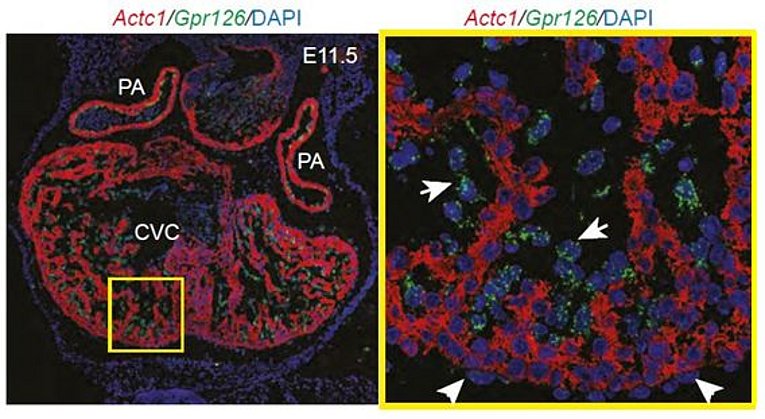
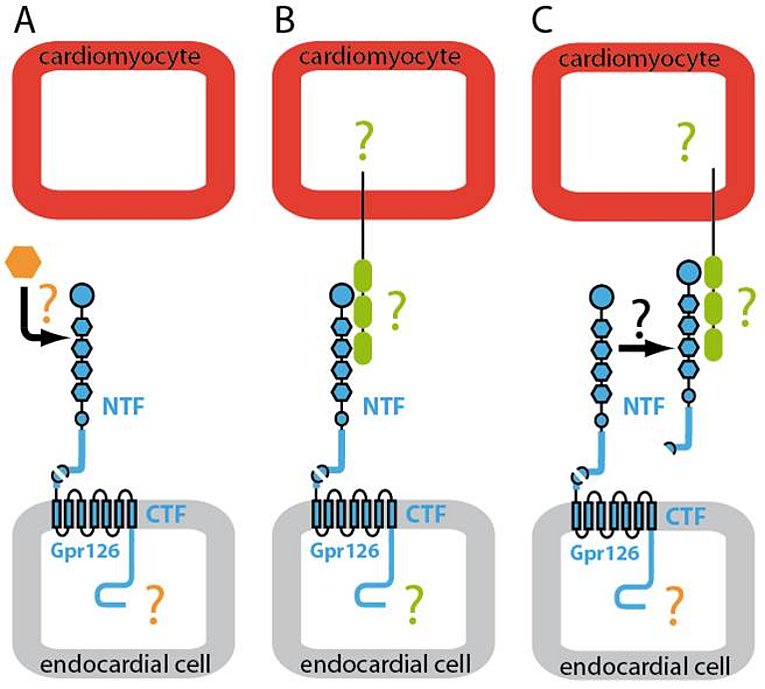
Wir konnten zeigen, dass die Funktion von Gpr126 für die Herzentwicklung notwendig ist. Das Fehlen oder Stilllegen von Gpr126 verursacht mitochondriale Dysfunktion und ventrikuläre Hypertrabekulation bei Mäusen und Zebrafischen. Mithilfe von Domän-spezifischen Morpholinos im Zebrafisch, Rettungsexperimenten in Gpr126-Morphanten und einem in situ Protein-Bindungs-Assay unter Verwendung von mGpr126-NTF auf Maus-Gewebeschnitten haben wir gezeigt, dass das NTF-Fragment von Gpr126 für die Herztrabekulation wichtig ist. Unsere Daten deuten darauf hin, dass mGpr126-NTF auf parakrine Weise wirkt. Allerdings bleibt der molekulare Mechanismus, welcher von Gpr126 zur Regulation der Herzentwicklung genutzt wird, unklar. Deshalb arbeiten wir an folgenden Fragestellungen:
- Identifikation von molekularen Veränderungen des Herz-Phänotypen von Gpr126 Knockout Mäusen
- Charakterisierung Zelltyp-spezifischer Deletion von Gpr126 in konditionalen Gpr126 Knockout Mäusen
- Erstellen von Zellsystemen, um die Funktion und nachgeschaltete Signaltransduktionswege von Gpr126 zu analysieren
- Struktur-Funktions-Analysen von Gpr126 im Zebrafisch
- Identifizierung von Bindungspartner von NTF-Gpr126